作者向本刊投稿即视为同意本刊对文章进行编辑、刊登和数字化发行。为适应我国信息化建设,扩大本刊及作者知识信息交流渠道,本刊被《中国学术期刊网络出版总库》及中国知网(CNKI)独家收录。如作者不同意文章被以上数据库收录,请在来稿时向编辑部声明,本刊将做适当处理。
|
微波萃取在土壤SVOCs分析中的应用与研究时间:2024-08-05 陈洪声,陈梅梅*,陈思帆,田光雨 (贵州省化工研究院,贵州 贵阳 550000) 摘 要:本文通过微波萃取与传统的索氏提取、加压流体萃取方法进行对比,探索微波萃取(MAE)技术用于土壤半挥发性有机物萃取的实验方法。研究结果探讨了时间、温度对微波萃取技术的影响,确定最优的萃取条件参数,采用实际土壤样品,从萃取有机组分含量上对微波萃取、加速溶剂萃取和传统索氏提取进行了方法比较,微波萃取SVOCs的相对丰度、色谱-质谱特征、标准要求的参数指标结果均与加压流体萃取以及经典的索氏萃取的结果相一致,实验结果表明,可有效地应用于SVOCS化学分析测试及样品前处理。 关键词:微波萃取法;土壤;半挥发有机物;研究
基金项目: 1、贵州省科技计划项目 蛋鸡规模养殖粪污生物发酵技术研究 (黔科合支撑[2023]一般017) 2、玉米秸秆高温发酵过程中氮损失关键影响因素研究(黔科院J字(2023)10号) 作者:陈洪声(1999-3),男,贵州贵阳,本科,助理工程师,从事分析检测。 通讯作者:陈梅梅(1997-1),女,贵州遵义,本科,助理工程师。
Application and research of microwave extraction in soil SVOCs analysis CHEN Hong-sheng,CHEN Mei-mei,CHEN Si-fan,TIAN Guang-yu (Guizhou Institute of Chemical Engineering, Guiyang, Guizhou,550000) Abstract: This article compares microwave extraction with traditional Soxhlet extraction and pressurized fluid extraction methods to explore the experimental method of microwave extraction (MAE) technology for extracting semi volatile organic compounds from soil. The research results explored the effects of time and temperature on microwave extraction technology, determined the optimal extraction condition parameters, and compared the methods of microwave extraction, accelerated solvent extraction, and traditional Soxhlet extraction from the content of organic components extracted from actual soil samples. The relative abundance, chromatography-mass spectrometry characteristics, and The parameter index results required by the standard are consistent with the results of pressurized fluid extraction and classical Soxhlet extraction. The experimental results show that it can be effectively applied to SVOCS chemical analysis testing and sample pretreatment. Key words:Microwave extraction ; soil ; Semi-volatile organic matter ; research,application
引言 土壤半挥发性有机物污染开始引起人们的重视[1-2],已经成为许多家不可缺少的监测内容,半挥发有机物指的是沸点在 170-350 摄氏度、蒸气在(0.1~10-7)×133.322 pa 之间的有机物[3],如今比较常见的半挥发有机物有苯系物、苯酚类、硝基芳香烃类、多环芳烃和有机氯农药。它们对人体的皮肤、神经系统[4]、眼睛、内分泌系统、呼吸系统、生殖系统都会造成严重的损伤[5],因此对土壤中SVOCs测定研究,对了解环境污染状况有重要意义。传统的提取方法有索氏提取和超声波法提取,他们明显都存在着提取的时间过长、需要萃取溶剂过多、回收率较低、精确度不好等缺点。微波萃取是相对比较年轻的萃取方法[6],Silgoner[7]研究表明微波萃取 3 min 相当于索氏提取 6 h,溶剂用量节约了 12~30倍[8],对于最传统的提取方法—索氏提取具有快速、高效、操作便捷、安全、回收率较高、所需溶剂少等优越性,减轻了分析工作者的工作强度,得到了广大分析工作者的青睐。随着国内外分析工作者的深入研究,现如今此技术已经广泛的应用于药物的提取、环境监测,在食品分析[9],化工分析[10],中草药有效成分的提取[11]都有广泛的应用。 1 实验仪器与试剂 主要仪器:气相色谱质谱联用仪(GC/MS):Agilent 6890 Serirs GC System ,色谱柱:AB-5MS(30m×0.25mm×0.25mm),微波萃取仪:MDS-6G,氮吹仪:JC-WD-12(S),索氏提取器:经典式玻璃索氏提取装置。 主要试剂:半挥发有机物标准储备溶液(购买):质量浓度为2000 ppm(2-氯苯酚、萘、硝基苯、苯并[a]蒽屈、苯并[b]荧蒽、苯并[k]荧蒽、苯并[a]芘、茚并[1,2,3-cd]芘、二苯并[a,h]蒽),替代物标准储备溶液(购买):质量浓度为4000 ppm(苯酚-d6,2-氟苯酚,2,4,6-三溴苯酚,硝基苯-d5,2-氟联苯,4,4’-三联苯-d14),内标储备溶液(购买):质量浓度为4000 ppm(1,4-二氯苯-d4,萘-d8,厄-d10,菲-d10,屈-d12,苝-d12),二氯甲烷(色谱纯)、丙酮(色谱纯),无水硫酸钠(400度烘4h,冷却装瓶保存)、玻璃纤维滤膜。 2 微波萃取条件的筛选 2.1 萃取温度 分别准确称取 10.00g 高温烘过石英砂8份,将8份试样分成四组,以二氯甲烷丙酮(1:1)为萃取溶剂,分别在其中加入 100μL 半挥发有机物标准使用液(100 μg/mL),此时试样的含量为 1.0mg/kg,在相同时间 30min下,在,60℃、90℃、120℃、130 ℃温度下进行萃取。几种温度下的加标回收率分别为 52%~60%,68%~94%,50%~83%,33%~89%。 2.2萃取时间 分别准确称取 10.00g 高温烘过石英砂6份,将6份试样分成三组,分别在其中加入 100μL 半挥发有机物标准使用液,此时试样的含量为 1.0 mg/kg,在相同温度下120 ℃下,分别在15 min、30 min、45 min下进行萃取。回收率分别为53%~81%,68%~94%,48%~90%。从以上得出微波萃取的最优萃取条件是90℃下萃取 30分钟。 3 样品的前处理 3.1 微波萃取 准确称取新鲜土壤 20.00 g,加入适量的无水硫酸钠混匀,对土壤进行脱水、研磨成小颗粒,装入微波消解杯中,加入 30 mL二氯甲烷-丙酮(1:1体积比)。加入适替代物,在功率为 8,温度 90℃ 下萃取 30 min,如果提取液中存在水分,需要进一步脱水,在漏斗上放上玻璃纤维滤膜,加入适量 400℃ 烘过的无水硫酸钠,将提取液过滤至浓缩器中,并用二氯甲烷-丙酮混合溶液(1:1体积比)洗消解杯3次,再用少量溶剂冲洗漏斗。用氮吹仪浓缩仪在 45℃ 下将提取液浓缩至 1 ml。根据 HJ-834[12]净化后,待上机测试。 3.2 索氏抽提提取法 准确称取实际土壤样品 ( 20. 0±0. 2) g,用滤筒包好后置于索氏提取器中。加入适替代物,在 500 m L 圆底烧瓶中加入 150 mL 二氯甲烷/丙酮( 1∶1) 土壤提取剂,加热回流18 h。之后浓缩定容至 1 mL。根据HJ-834[12]净化后,待上机测试。同时按相同方法提取空白样品。 3.3 加压流体萃取法 准确称取新鲜土壤 20.00 g,加入适量的无水硫酸钠混匀,对土壤进行脱水、研磨成小颗粒,加入 80μl 替代物中间液(100ppm),将玻璃纤维滤膜置于洗净萃取池的底部,将试样填入萃取池。平稳放入加压流体萃取装置,设置萃取条件,启动仪器后,待萃取结束后,将接收瓶中的萃取液用氮吹仪在常温下浓缩至 1ml。根据 HJ-834[12] 净化后,待上机测试。同时按相同方法提取空白样品。 3.4 气相色谱质谱法上机分析 进样口温度:300℃,不分流。进样量:1μL,柱流量:1.0 mL/min(恒流),柱温:35℃开始保持两分钟,以15℃/min升温至150℃,保持5min,以3℃升温至300℃,保持两分钟。离子源温度:230℃,接口温度:280℃,四级杆温度:150℃,质量扫描范围:35~450u,溶剂延迟时间:5min。 3.4.1 气相色谱条件 表3-1气相色谱条件 Table 2-1 Gas chromatographic conditions
3.4.2 质谱条件 表3-2 质谱条件 Table 2-2 Mass spectrometric conditions
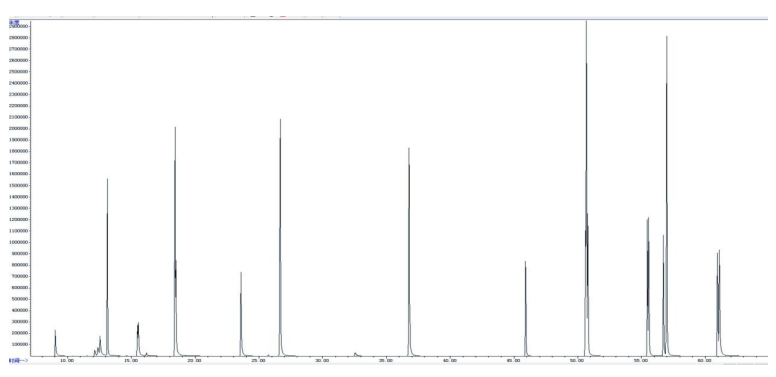
按照此分析条件下的升温程序可从图3-3中可以看到各组分基本分离,分析一个样品需要65分钟。
图3-3 11种半挥发有机物总离子图(SIM) 4 结果与讨论 4.1 标准曲线 11中半挥发有机物在1、4、8、10、20 μg/mL浓度梯度下的标准曲线和相关关系见表1。 表1 VOCs标准曲线
4.2 检出限 重复分析 7 个标准样品,计算其标准偏差(S)、相对标准偏差(RSD),仪器检出限(MDL)=3.14S。结果见表2。
表2 各方法检出限
4.3 不同前处理空白加标回收率 三种不同的提取方法下,空白样品加标回收率的结果见表3
表3 准确度和精密度实验结果
5 结论 本文探索了微波萃取对土壤中半挥发有机物的萃取实验方法,确定了最优的萃取条件参数为时间:30 min、温度:90 ℃、萃取溶剂为二氯甲烷丙酮溶液。进行方法的重现性实验,萃取结果具有很好的精密度和加标回收率,相对标准偏差(RSD)在 6~13%。回收率在 68%~95% 之间。采用土壤样品,从萃取有机组分的含量上对微波萃取与加速溶剂萃取和传统索氏提取进行了方法比较,采用 6 个土壤样品进一步对SVOCs中的标志物进行了对比,微波萃取SVOCs的相对丰度、色谱-质谱特征、标准要求的参数指标结果均与加压流体萃取以及经典的索氏萃取的结果相一致,实验结果表明, 微波萃取技术在时间和回收率以及检出限上优于其他2种萃取技术,可有效地应用于SVOCS化学分析测试及样品前处理.并且具有回收率较高、操作简单、样品提取时间短、可以大批量处理样品,溶剂用量少等独特的优点。还很大程度上降低了分析人员的工作 强度,全程密闭对环境污染小等特点,本文初步建立了微波萃取-GC/MS法测定土壤中SVOCs的方法。对土壤中SVOCs的测定研究具有一定的意义。 参考文献: [1] Sun C,Zhang J,Ma Q,et al. Environmental Geochemistry and Health[J]. Environmental Geochemistry and Health,2017,39: 63. [2] Wang Y,Luo C L,Wang S R,et al. Environmental Science andTechnology[J]. Environmental Science and Pollution Research International,2015,49( 1) : 284-291. [3] 吕天峰,张宝,滕思江等.固相微波萃取-气象色谱质谱法测定水中半挥发性有机污染物[J].理化检验化学分册,2013,49(8):957-960. [4] 张焕珠,宋伟民.挥发性有机物对小鼠神经行为功能的影响[J].环境与职业医学,2005,22(2):112-115. [5] 丁宝国.土壤中典型半挥发有机污染物柱净化-串联质谱分析方法研究[D].南京农业大学,2014. [6] 潘学军,刘会洲.微波辅助提取(MAE)研究进展[J]化学通报.1999,(5):7. [7] Silgoner I, Krsha R, Lombas E, Gans O, Rosenberg E, Grasserbauer M. Freseniu S, J.Anal. Chem.[J],1998,362(1):120. [8] Mcmillin R,Miner L c,Hurst L.Abbreviated microw are extraction of pesticides and PCB in soi[J].Spectroscopy,1997,13(1):41~50. [9] 高彦祥.微波萃取技术及其在食品工业中的应用[J].食品与机械,1998,(2):38-39. [10] 王小强,代木日勒.微波萃取技术及其应用[J].福建质量管理,2017,(10). [11] 傅荣杰,冯怡.微波萃取技术中药及天然产物提取中的应用[J].中国中药杂志,2003,28(9):804. [12] 环境保护部.HJ834-2017土壤和沉积物半挥发性有机物的测定.气相色谱-质谱法[S].北京:中国环境科学出版社,2017. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||