зїепЯђБОПЏЭЖИхМДЪгЮЊЭЌвтБОПЏЖдЮФеТНјааБрМЁЂПЏЕЧКЭЪ§зжЛЏЗЂааЁЃЮЊЪЪгІЮвЙњаХЯЂЛЏНЈЩшЃЌРЉДѓБОПЏМАзїепжЊЪЖаХЯЂНЛСїЧўЕРЃЌБОПЏБЛЁЖжаЙњбЇЪѕЦкПЏЭјТчГіАцзмПтЁЗМАжаЙњжЊЭјЃЈCNKIЃЉЖРМвЪеТМЁЃШчзїепВЛЭЌвтЮФеТБЛвдЩЯЪ§ОнПтЪеТМЃЌЧыдкРДИхЪБЯђБрМВПЩљУїЃЌБОПЏНЋзіЪЪЕБДІРэЁЃ
|
ЬНОПЯћЛЏЪБГЄЖдЗЪСЯзмЕЊЕФгАЯь时间ЃК2024-08-05 ГТУЗУЗЃЌГТКщЩљЃЌДњгІЛс ЃЈЙѓжнЪЁЛЏЙЄбаОПдКЃЌЙѓжн Йѓбє 550002ЃЉ еЊ вЊЃКЫцзХХЉвЕЕФВЛЖЯЗЂеЙНјВНЃЌШЫУЧЖдЗЪСЯЕФМьВтвЊЧѓвВдНРДдНИпЃЌЙигкЗЪСЯжазмЕЊКЌСПЕФМьВтвВЪЎЗжжиЪгЃЌБОЮФгУФђЫибљЦЗВтЪдЕЊКЌСПЃЌЬНОПКьЭтжЧФмЯћЛЏТЏЖдЗЪСЯзмЕЊКЌСПВтЖЈЕФЯћжѓЪБГЄНјааЪЕбщЗжЮібаОПЃЌЭЌЮТЖШЯТЃЌЗжВЛЭЌЪБМфЖЮПЊеЙЪЕбщЃЌМьВтЪ§ОнНсЙћЕУГіЃЌЯћжѓЪБГЄДяЕН 3h-3.5hЃЌИїжжаЮЪНЕФЕЊШЋВПзЊЛЏЮЊяЇЬЌЕЊЃЌМДЕЊЯћЛЏЙ§ГЬШЋВПзЊЛЏЭъГЩЁЃЦфжаЯъЯИУшЪіЪЕбщЙ§ГЬжаГіЯжЕФИїжжЮЪЬтвдМАЪЕбщЙ§ГЬжагІИУзЂвтЪТЯюНјааСЫВћЪіЁЃБОЮФЖдЗЪСЯЁЂжВжъЁЂЭСШРВтЖЈЕЊКЌСПЯрЙиМьВтЬсЙЉВЮПМЃЌЪЙзмЕЊКЌСПЕФМьВтЪ§ОнИќМгзМШЗЁЃ ЙиМќДЪЃККьЭтжЧФмЯћЛЏТЏЁЂФђЫиЁЂзЂвтЪТЯю ЛљН№ЯюФП1ЃКЙѓжнЪЁПЦМММЦЛЎЯюФП ЕАМІЙцФЃбјжГЗрЮлЩњЮяЗЂНЭММЪѕбаОП ЃЈЧПЦКЯжЇГХ[2023]вЛАу017ЃЉ ЛљН№ЯюФП2ЃКгёУзНеИбИпЮТЗЂНЭЙ§ГЬжаЕЊЫ№ЪЇЙиМќгАЯьвђЫибаОП ЧПЦдКJзж (2023) 10КХ зїепЃКГТУЗУЗЃЈ1997-ЃЉЃЌХЎЃЌЙѓжнзёвхШЫЃЌБОПЦЃЌжњРэЙЄГЬЪІЃЌжївЊбаОПЗНЯђЃКаТаЭТЬЩЋЗЪСЯгыЛЗОГБЃЛЄЁЃ ЭЈбЖзїепЃКГТКщЩљЃЈ1999-ЃЉЃЌФаЃЌЙѓжнЙѓбєШЫЃЌБОПЦЃЌжњРэЙЄГЬЪІЁЃ
Abstract: With the development of agriculture, the requirement of fertilizer detection is more and more high, and the detection of total nitrogen content in fertilizer is also very important, in order to study the digestion time of the determination of total nitrogen content in fertilizer by infrared intelligent digester, the experiment was carried out at the same temperature and in different time periods, all forms of nitrogen are converted into ammonium nitrogen, that is, nitrogen digestion process is completed. It describes in detail the various problems in the experimental process and the matters needing attention in the experimental process. This paper provides a reference for the determination of nitrogen content in fertilizer, plant and soil, and makes the determination data of total nitrogen content more accurate Keywords: infrared intelligent digestion furnace, urea, notes ЫцзХЮвЙњХЉвЕбИЫйЗЂеЙЃЌЦфжаХЉвЕЩњВњжаЃЌЖдЗЪСЯзмЕЊКЌСПЕФМьВтдНРДдНжиЪгЁЃЗЪСЯзмЕЊМьбщЙ§ГЬБШНЯИДдгЃЌЪБМфНЯГЄЁЃЪЕМЪВйзїЙ§ГЬжавВЛсГіЯжИїжжЮЪЬтЃЌЖддРэВЛЧхГўЃЌвьГЃЕФЪ§ОнЮоДгХаЖЯДэЮѓИљдДЃЌВйзїЙ§ГЬВЛЙцЗЖЃЌЖдМьВтЪ§ОндьГЩЮѓВюЁЃвдЯТИљОнЪЕбщЪвВтЖЈЗЪСЯЕЊКЌСПЙ§ГЬжаЕФвЛаЉОбщЃЌНјааЯъЯИУшЪіЃЌгыДѓМвЙВЭЌВЮПМЃЌвЛЦ№бЇЯАЁЃ 1 ВЩгУЗНЗЈКЭЛљБОдРэ БъзМ GB/T 8572-2010 жаЗЪСЯзмЕЊВтЖЈЗНЗЈЪЧеєСѓЕЮЖЈЗЈЃЌдРэЃКдкМюадНщжЪжагУЖЈЕЊКЯН№НЋЯѕЫсИљЛЙд,жБНгеєСѓГіАБЛђдкЫсадНщжЪжаЛЙдЯѕЫсбЮГЩяЇбЮ,дкЛьКЯДпЛЏМСДцдкЯТЃЌгУХЈСђЫсЯћЛЏЃЌНЋгаЛњЬЌЕЊЛђѕЃАЗЬЌЕЊКЭЧшАБЬЌЕЊзЊЛЏЮЊяЇбЮЃЌДгМюадШмвКжаеєСѓАБЁЃНЋАБЮќЪедкЙ§СПСђЫсШмвКжаЃЌдкСђЫсМиКЭСђЫсЭЛьКЯжИЪОМСДцдкЯТЃЌгУЧтбѕЛЏФЦБъзМШмвКЗЕЕЮЖЈЁЃ ЗЪСЯжаЕЊДцдкЕФаЮЪНвЛАувдЯѕЬЌЕЊЁЂгаЛњЕЊЁЂѕЃАЗЬЌЕЊЕШДцдкЁЃЖдгкКЌгаЛњЕЊЕФЗЪСЯЃЌШчФђЫиЕШгаЛњЗЪЃЌВЩгУЕФЪЧКьЭтжЧФмЯћЛЏТЏИпЮТЯћжѓЃЌПЪЯЖЈЕЊвЧеєСѓЁЃдРэЪЧЃКдкСђЫсЭКЭСђЫсМиЕФЛьКЯДпЛЏМСзїгУЯТЃЌгУХЈСђЫсЦЦЛЕЪдбљжаЕФКЌЕЊЮяжЪЃЌЪЙКЌЕЊЮяжЪзЊЛЏГЩСђЫсяЇЃЌШЛКѓЭЈЙ§МгМювКеєСѓВтЖЈзмЕЊКЌСПЁЃЖдгкжЛгаяЇЬЌЕЊЕФВЛашЯћжѓЃЌПЩвджБНгеєСѓЁЃ 2 ЪЕбщВНжш
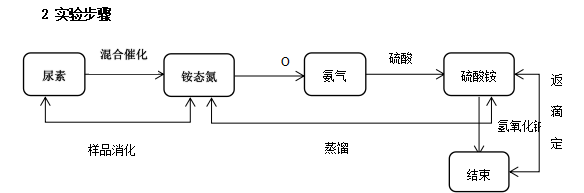
3 ЪЕбщЙ§ГЬ ВЩгУБъзМ GB/T 8572-2010 жаНјааЪЕбщбщжЄЃЌвдФђЫиЮЊвбжЊКЌСПЪдбљЁЃдкЯћжѓЙмжаМгШыГЦКУЕФФђЫиЃЌМгШы 10g СђЫсЭКЭСђЫсМиЛьКЯДпЛЏМСЃЌвРДЮМгШы 20mL ХЈСђЫсЃЌЗХШыКьЭтжЧФмЯћЛЏТЏНјааЯћжѓЃЌНЋЯћжѓЙмНјааБрКХЃЈ1-18КХЃЉЃЌЮТЖШКуЖЈ 350Ёц жЎКѓЃЌ1-3КХЯћжѓЙмЯћжѓ2hКѓШЁГіРфШДЃЌ4-6КХЯћжѓЙмЯћжѓ2.5hКѓШЁГіРфШДЃЌ7-9КХЯћжѓЙмЯћжѓ3hКѓШЁГіРфШДЃЌ10-12КХЯћжѓЙмЯћжѓ3.5hКѓШЁГіРфШДЃЌ13-15КХЯћжѓЙмЯћжѓ4hКѓШЁГіРфШДЃЌ16-18КХЯћжѓЙмЯћжѓ5hКѓШЁГіРфШДЃЌШ§ИіЪЕбщЪвПеАзЃЈВЛМгФђЫиЃЉЃЌЪЕбщПЊЪМжЎЧАБиаыЬсЧАДђПЊРфШДЫЎЃЌдкЭЈЗчГїФкНјааЁЃ 4 ЪЕбщВйзїЙ§ГЬжазЂвтЪТЯю 4.1 Яћжѓ дкЯћжѓЙ§ГЬжаЃЌИеПЊЪМЮТЖШВЛвЫЙ§ИпЃЌЮДжЊбљЦЗжаПЩФмКЌгаДѓСПЬЧЗжЃЌИпЮТЙ§ГЬжаВњЩњДѓСПЦјХнвчГіЁЃМгШШЪБЯШМгШШЕН 200Ёц МАвдЯТЃЌЪЙХнФж№НЅЯћЪЇЃЌдкЕїЮТЕН 250ЁцЁЂ300Ёц ж№НЅЩ§ЮТЕН 350Ёц зѓгвМДПЩЃЌЮТЖШвВВЛвЫЙ§ИпЃЌЙ§ИпЛсЪЙВПЗжЕЊЛгЗЂЖЊЪЇЃЌЕМжТЪ§ОнЦЋЕЭЃЌМгШШжСУАСђЫсАзбЬЃЌГЪЛиа§зДЁЃвЛИіаЁЪБжЎКѓЙмФкбеЩЋБфГЩРЖЩЋШмвКЧвЭИССЃЌЯћжѓЪБМфдк2hЁЂ2.5hЁЂ3hЁЂ3.5hЁЂ4hЁЂ5h вРДЮШЁГіЁЃзЂвтЃЌШЁГіЯћжѓЙмЪБзЂвтАВШЋЃЌЯШЙиЛ№ЃЌДјПкежЃЌЗРЬЬЪжЬзЃЌШЁГіКѓЛЛЩЯМгЩйСПЕФ 2-4mL ХЈСђЫсЕФЯћжѓЙмЃЌНїЗРЯћжѓТЏгаПеЮЛЪмШШВЛОљеЈСбЃЌвВБЃЛЄПеЙмдкИпЮТЯТВЛЛсеЈСбЃЌМЬајЯћжѓЃЌжБЕНзювЛИљЯћжѓЭъЁЃШЁГіЯћжѓЙмЗХжУЪБМфВЛвЫЙ§ГЄЃЌЪБМфЙ§ГЄРяУцЕФвКЬхЛсеГГэдквЛЦ№ЃЌдкПЪЯеєСѓзАжУЩЯВЛКУВхЙмЯћжѓЃЌШчЙћЮТЖШЙ§ИпОЭЗХжУгкЖЈЕЊвЧЩЯЛсЬЬЛЏЖЈЕЊвЧЕзВПЃЌЪЙЯћжѓЙмРфШДжСВЛЬЬЪжМДПЩНјааеєСѓЁЃ 4.2 еєСѓ ЯШДђПЊЫЎдДЃЌПЊЦєПЪЯЖЈЕЊвЧЯШНјаадЄШШДѓИХАыаЁЪБЃЌзАСЫЩйСПЫЎЕФЯћжѓЙмНјааеєСѓСНЕНШ§ДЮЃЌЪЙвЧЦїДІгкМюадЛЗОГЯТЃЌж№НЅЧїгкЮШЖЈЃЌетбљВйзїЕФФПЕФЃЌВХФмНЋбљЦЗжаЕФяЇЬЌЕЊШЋВПзЊЛЏЮЊАБЦјЃЌИќгааЇЕФБЛСђЫсШмвКЮќЪеЃЌзЊЛЏЮЊСђЫсяЇЃЌЪ§ОнИќМгзМШЗгааЇЁЃЫцКѓдкБрКХЕФЯћжѓЙмжаМгШыЬхЛ§ЮЊ 80mLЃЌХЈЖШЮЊ 400g/ LЧтбѕЛЏФЦШмвКЃЌдкМюадЛЗОГЯТЖдбљЦЗНјааеєСѓЁЃШчЙћЗДгІЙ§ГЬжаЯћжѓЙмФкШмвКГЪРЖЩЋЃЌМДМюадЬѕМўВЛЙЛЃЌМЬајЬэМгМювКЃЌУПДЮ 10mLЃЌжиаТЕїећвЧЦїеєСѓЪБМфЁЃжБЕНЯћжѓЙмФкШмвКБфКкВХФмТњзуЗДгІЬѕМўЁЃЃЈдРэЃКСђЫсЭжаЕФЭРызгдкЙ§СПЧтбѕЛЏФЦШмвКЕФЬѕМўЯТЃЌЩњГЩвЛжжШмвКжаДцдкзХгЩЖўМлЭРызгзїжааФдзгєЧЛљзїХфЬхЕФЫФєЧЛљКЯЭХфКЯРызгЁЃМгМюдіЧПШмвКЕФМюадФмдіЧПШмвКЕФЮШЖЈадЃЌЕЋМДЪЙЪЧЫФєЧЛљКЯЭЫсФЦЕФИпХЈЖШМюШмвКЃЌЦфОУжУЪ§жмжСЪ§дТШдФмМћЕНВПЗжКкЩЋбѕЛЏЭГСЕэЁЃФПЧАЩаЮДШЗЖЈЫФєЧЛљКЯЭЫсФЦЪЧЗёгаЙЬЬхбЮДцдкаЮЪНЁЃЗДгІЗНГЬЪНШчЯТЃК CuSO4+2NaOH==Cu(OH)2+Na2SO4 ЃЌНјвЛВНЗЂЩњТчКЯЗДгІЃК 4.3 ЕЮЖЈ БОЪЕбщЪвЪЧвЛИіЗЕЕЮЖЈЕФЙ§ГЬЃЌЫљвдПеАзЕЮЖЈЯћКФБъзМШмвКЕФСПБШбљЦЗЯћКФБъзМШмвКЕФСПвЊЖрЃЌБъзМШмвКЪЙгУЧАвЊНјааБъЖЈЃЌБЃСєЫФЮЛаЁЪ§ЕуЃЛУПЕЮЖЈЭъвЛИібљЦЗЃЌжиаТаЃСуЃЌБмУтЖСЪ§ЮѓВюЖдЪ§ОндьГЩгАЯьЁЃЃЈзЂвтЃКОпШћЕЮЖЈЙмЕїСуЃЌХХЦјХнЃЌзёб GB/T 601-2016 ЕЮЖЈЫйЖШЃЈ6mL-8mLЃЉ/min МДПЩЃЉ 5 Ъ§ОнНсТлМАОбщзмНс ИљОнЙЋЪН
Бэ5-1ЮТЖШКуЖЈдк350ЁцзѓгвАДВЛЭЌЪБМфЖЮШЁГі 5.1 Ъ§ОнНсТл Бэ5-2ЯћжѓЪБГЄЖдгІЕЊКЌСПЪ§ОнЭМ
ИљОнБэ5-2жаЪЕбщЪ§ОнНсЙћЙцТЩгыФђЫиРэТлЕЊКЌСП 45-46% ПЩЭЦЖЯГіЃЌЮТЖШДяЕНЮШЖЈКѓЃЌФђЫиЕФЯћжѓЙ§ГЬдк 3h КѓОЭЧїгкЦНКтЃЌДЫЪБЯћНтЛљБОЭъГЩЃЌЕЋГігкЖдФђЫижаКЌгаЩйСПдгжЪЃЌЕЊКЌСПЛсБШРэТлжЕаЁЁЃЖдгкЪЕМЪбљЦЗРДЫЕЃЌгааЉЕЊЕФаЮЬЌБШНЯФбзЊЛЏГЩяЇЬЌЕЊЃЌЫљвдЯћжѓЭЈГЃЪБМфЛсБШНЯОУЁЃ3h-3.5h ЕФЯћжѓОЭФмАбЕЊКЌСПШЋВПзЊЛЏГЩяЇЬЌЕЊЁЃ 5.2 ОбщзмНс 5.2.1 ГЦШЁЪдбљ ГЦШЁЪдбљКЯРэЃЌ0.5g зѓгвМДПЩЁЃШчЙћГЦбљСПЙ§ЖрЃЌЖдгкЕЊКЌСПИпЕФбљЦЗЃЌПЩФмЛсЕМжТдкеєСѓЙ§ГЬжаЃЌеєСѓГіЕФЕЊКЌСПЙ§ЖрЃЌЮќЪевКВЛзуЃЌЮќЪеВЛЭъШЋЃЌдьГЩЕЊКЌСПЕФЫ№ЪЇЃЌЪЙНсЙћЦЋЕЭЃЛШчЙћГЦбљСПЩйЃЌЖдгкЕЊКЌСПЩйЕФбљЦЗЃЌПЩФмЛсЕМжТЕЮЖЈЙ§ГЬжаЃЌБъзМШмвКХЈЖШЦЋИпЃЌдьГЩХЈЖШЮѓВюЁЃ 5.2.2 ЯћжѓвЊГЙЕзЛКТ§Щ§ЮТ дкЯћжѓЙ§ГЬжаЃЌбљЦЗгыМгШыЕФЪдМСвЊЛьКЯОљдШЃЌЙ§ГЬжаЛКТ§Щ§ЮТЃЌЮТЖШЙ§ИпПЩФмгаДѓСПЦјХнвчГіЃЌПЩФмЛсЕМжТбљЦЗЫцзХЦјХнХмГіЃЌбљЦЗСїЪЇЃЌЪЙЕЊКЌСПЦЋЕЭЕШЁЃЯћжѓЙ§ГЬжазЂвтЙлВьбеЩЋБфЛЏЃЌШЗБЃНЋШЋВПЕЊКЌСПзЊЛЏЮЊяЇЬЌЕЊЕФаЮЪНЃЌЗёдђЛсдьГЩНсЙћЦЋЕЭ[1]ЁЃ 5.2.3 ЪЕбщПеАзвЊМьВт дкЪЕбщЙ§ГЬжаЃЌПеАзжЕвЊдкБъзМвЊЧѓЗЖЮЇФкЪЧБЃжЄМьВтНсЙћзМШЗадЕФЧАЬсЁЃПеАзЦЋИпЃЌЪЧЪВУДдвђЪмЕНЪВУДЮлШОЕМжТЦЋИпЃЌгІМАЪБВщевдвђНтОіЮЪЬтРДдДЃЌЬНОПЪЧВЛЪЧЪдМСДПЖШВЛЙЛЃЌЪЧЗёЪЕбщЪвЫЎВЛДПОЛЃЌдкЪЕбщЙ§ГЬжаЪЧЗёгаЦфЫћдгжЪНщШыЕМжТЮлШОЃЌЪЙгУВЃСЇвЧЦїЪЧЗёУЛгаГхЯДИЩОЛЕШдвђНјааМАЪБЗжЮіДІРэ[2-3]ЁЃ 5.2.4 зіКУЦНаабљЦЗМьВт ЪЕбщЙ§ГЬжаВЩШЁЦНаабљПижЦЪжЖЮЃЌгІДгГЦбљПЊЪМЃЌЦНаабљГЦбљСПВЛвЫЯрВюЬЋДѓЃЌОЁСПБЃГжвЛжТЁЃШЗБЃМьВтНсЙћЪЧЗёКЯРэЃЌЦНааВтЖЈНсЙћгІТњзуБъзМЦНааЦЋВюЗЖЮЇжЎФкЃЌМьВтНсЙћЗНПЩКЯИёЁЃМьВтбљЦЗЙ§ЖрПЩЖрзіМИзщЦНаабљЁЃ 5.2.5 ЕЮЖЈгУЕФБъзМШмвКвЊБъЖЈ ЖдгкЕЮЖЈЛЗНкЃЌШЮКЮБъвКдкЪЙгУжЎЧАЖМвЊЖдИУШмвКЕФХЈЖШНјааБъЖЈЃЌВЂЧвБъЖЈХЈЖШгыХфжУЕФЪЕМЪХЈЖШЯрЖдЮѓВюВЛФмГЌГі ЁР5%ЃЌЗДжЎЃЌИУХЈЖШгІжиаТХфжУЃЌЪЙгУЧАНЋШмвКЦПЩЯЯТвЁЖЏМИДЮЃЌЪЙШмвКГфЗжЛьдШЃЌХЈЖШОљдШБЃГжвЛжТЁЃЕЮЖЈЪБзЂвтХХГ§ЕЮЖЈЙмЕзВПЕФЦјХнЃЌШЗБЃЕЮЖЈНсЙћзМШЗ[4-5]ЁЃ 6 зЂвт БъзМ GB/T 8572-2010 жаЙцЖЈЛьКЯжИЪОМСЮЊ 22gЃЌХЈСђЫсЮЊ 30mLЃЌЧтбѕЛЏФЦШмвКЮЊ120mLЃЌЕЋдкБОЮФжаЛьКЯжИЪОМСЪЙгУСПЮЊ 10gЃЌХЈСђЫс 20mLЃЌЧтбѕЛЏФЦШмвКЮЊ 80mLМДПЩЃЌгыБъзМжаЯрБШДѓДѓЕФМѕЩйдБОвЉЦЗЪдМСЕФЪЙгУСПЁЃ ВЮПМЮФЯзЃК [1] ХЃезКь.ШчКЮЬсИпЗЪСЯжазмЕЊВтЖЈЕФзМШЗЖШ[J].ЯжДњЛЏХЉвЕ,2007(03):25-26. [2] еХЗЩСњ. .КьЭтжЧФмЯћЛЏТЏЕФгХдНад[J].ДѓжкБъзМЛЏ,2022,No.377(17):121-123. [3] бІУє,ЕЋЪЫгТ.ПЪЯеєСѓЗЈВтЖЈЭСШРШЋЕЊгІзЂвтЕФЪТЯюМАОбщзмНс[J].ХЉММЗўЮё,2017,34(09):58+57. [4] жмбр,еХго,ЬЗмчЕШ.БъзМЕЮЖЈШмвКДЂДцгааЇЦкбаОП[J].ЫФДЈЛЏЙЄ,2023,26(02):37-39. [5] ГТЗяЯМ,жмЯўУє,СѕУчУчЕШ.бЮЫсЕЮЖЈвКХфжЦБъЖЈЕФЗНЗЈ[J].жаЙњвЉЮяОМУбЇ,2023,18(03):92-94+100.
|

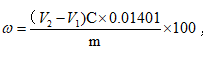 ЃЌМЦЫуНсЙћШчЯТЃК
ЃЌМЦЫуНсЙћШчЯТЃК